 更新时间:2026-02-13
更新时间:2026-02-13 点击次数:
点击次数:
YYVIP易游·(中国有限公司)官方网站-,是最具代表性的药食同源中药材之一。山楂经不同方法炮制后功效产生差异,其中焦山楂长于消食化积、止痢,并阐明其变化规律,是实现焦山楂炮制工艺科学优化与质量精准控制的核心前提。
传统的炮制工艺多依赖经验传承,缺乏系统的科学数据支撑,这不仅制约了山楂药效的稳定发挥,也影响了其在现代中药制剂中的应用与推广[2]。为实现焦山楂饮片质量的稳定可控,并突破传统工艺对主观经验的依赖,本研究将Q-Marker-热分析技术-电子感官技术相整合,对焦山楂炮制工艺进行系统研究,为山楂炮制品的标准化提供参考。
Waters-e2695型高效液相色谱仪,美国Waters公司;Diamonsil C18色谱柱(250 mm×4.6 mm,5μm),北京迪科马科技有限公司;SYU-10-300DT型超声波清洗机,郑州生元仪器有限公司;STA449-F5型热重-差热同步热分析仪,德国耐驰仪器制造有限公司;AR223CN型分析天平,美国奥豪斯公司;DE-100 g型万能高速粉碎机,浙江红景天工贸有限公司;GZX-9140MBE型电热鼓风干燥箱,上海博迅医疗生物仪器股份有限公司医疗设备厂;HH-2型水浴锅,北京科伟永兴仪器有限公司;YR-PTB型真空泵,上海亚荣生化仪器厂;ABL型系列多功能炒药机,兰州阿泊罗电子设备有限责任公司,规格25 L,投料量≥50 g;FD-1-50型冷冻干燥机,北京博尔康科技有限公司。
山楂饮片,产地信息见表1,由山西中医药大学中药与食品工程学院张朔生教授鉴定,基原均为蔷薇科山楂属植物山里红C.pinnatifidaBge. var.majorN. E. Br.的干燥成熟果实。
2.1.1焦山楂饮片的制备采用ABL系列多功能炒药机,按照《中国药典》2025年版四部通则“0213炮制通则”项下清炒法分别对编号S1~S10的生山楂进行炒焦,炒制后的焦山楂对应编号为J1~J10。
2.1.2混合对照品溶液的制备取绿原酸、异槲皮苷、金丝桃苷、芦丁对照品适量,精密称定,置于10 mL量瓶中,加甲醇溶解并定容,制成质量浓度分别为绿原酸33.97 μg/mL、异槲皮素28.53 μg/mL、金丝桃苷61.06 μg/mL、芦丁11.82 μg/mL的混合对照品溶液。
2.1.3供试品溶液的制备取山楂粉末1 g(过三号筛),精密称定,置于50 mL锥形瓶中,加入20 mL甲醇,称定质量后超声(300 W、25℃)40 min,放冷后再次称定质量,甲醇补足减失的质量,摇匀,静置后取上清,0.22 μm微孔滤膜滤过,备用。
2.1.5精密度考察取“2.1.3”项下供试品溶液,按照“2.1.4”项下色谱条件连续进样6次,以3号峰(绿原酸)为参照峰(S),计算得到各共有峰相对保留时间的RSD<1%,相对峰面积的RSD<2%,结果表明该仪器精密度良好。
2.1.6稳定性考察取“2.1.3”项下供试品溶液,分别于制备后0、4、8、12、24 h进样测定,以3号峰(绿原酸)为参照峰(S),计算得到各共有峰相对保留时间的RSD<1%,相对峰面积的RSD<2%,结果表明供试品溶液在24 h内稳定性良好。
2.1.7重复性考察按照“2.1.3”项下方法平行制备6份供试品溶液,按照“2.1.4”项下色谱条件进行测定,以3号峰(绿原酸)为参照峰(S),计算得到各共有峰相对保留时间的RSD<1%,相对峰面积的RSD<2%,结果表明该方法重复性良好。
2.1.8指纹图谱的建立及相似度评价取生山楂和焦山楂饮片各10批,按照“2.1.3”项下方法制备各供试品溶液,按照“2.1.4”项下色谱条件进样测定,利用“中药色谱指纹图谱相似度评价系统”,分别以S1、J1号样品的色谱图为参照图谱,运用多点校正法和中位数法生成叠加图谱及对照指纹图谱(图1)。生山楂确认出14个共有峰,焦山楂确定出10个共有峰,且生山楂、焦山楂共同确定了10个共有峰,通过与混合对照品(图2)保留时间及色谱峰光谱信息比对,指认了绿原酸(3号峰)、芦丁(10号峰)、金丝桃苷(11号峰)、异槲皮苷(12号峰)4个成分。绿原酸是山楂的标志性成分,化学性质稳定。在本研究体系中,其色谱峰位置适中、峰形对称,是所有样品中稳定出现的共有峰,因此其被选定为方法学考察的参照峰。相似度评价结果见表2、3。10批生山楂(S1~S10)及10批焦山楂(J1~J10)的样品图谱与相应对照指纹图谱的相似度均>0.9,表明各样品间的差异较小,质量较稳定。
2.2.1聚类分析使用SPSS 26.0,以10批生山楂与10批焦山楂HPLC指纹图谱的共有峰峰面积为变量,以平方欧式距离(squared Euclidean distance)作为样本间距离的度量标准,采用组间连接法(between-groups linkage)作为聚类连接方法,对20批样品进行系统聚类分析(hierarchical cluster analysis)。聚类结果以树状图展示,结果见图3。当平方欧式距离为25时,生山楂与焦山楂被分为2大类,结果表明,焦山楂炮制前后化学成分存在一定差异,可通过指纹图谱各色谱峰峰面积对生山楂、焦山楂二者进行初步分类。
2.2.2主成分分析(principal component analysis,PCA)以10批焦山楂炮制前后HPLC指纹图谱的共有峰峰面积为变量,利用SIMCA-P14.1软件,进行PCA,PCA得分见图4。结果显示,生山楂与焦山楂样品相比较,在其主成分空间中的分布明显分为2大类,表明通过共有峰面积可将生山楂与焦山楂进行初步划分,生山楂经炮制后各化学成分均存在一定差异。
2.2.3偏最小二乘法-判别分析(partial least squares-discriminant analysis,PLS-DA)以10批山楂炮制前后样品HPLC指纹图谱的共有峰峰面积为变量,利用SIMCA-P14.1软件,进行PLS-DA建模分析,结果见图5,该模型的解释能力R2X=0.897、R2Y=0.996;预测能力Q2为0.993,结果表明该模型成功且具有较强的预测能力,可用于山楂生品及焦山楂样品的区分。
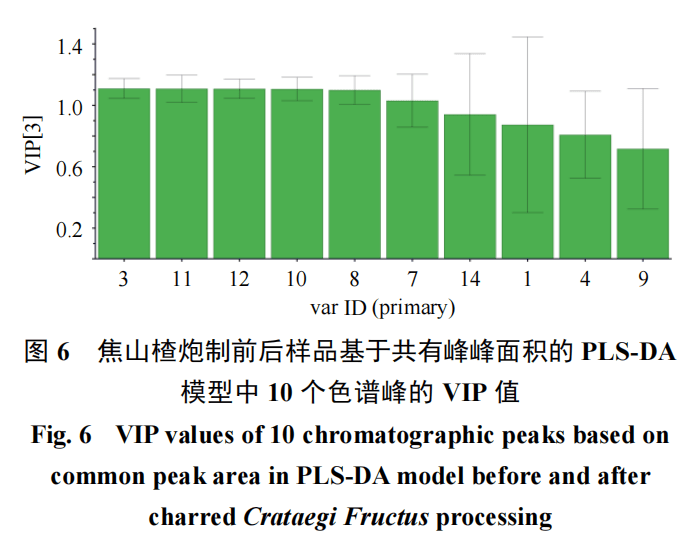
采用变量重要性投影(variable importance projection,VIP)值对其化学成分进行分析,VIP值大小与变量对于分类的贡献呈正相关,以VIP>1为筛选标准,共筛选出6个差异性显著的指标性成分。这些成分按其VIP值大小依次为峰3(绿原酸)>峰11(金丝桃苷)>峰10(芦丁)>峰12(异槲皮素)>峰8>峰7,结果见图6。
2.2.4山楂炮制前后差异性成分的筛选与确认基于山楂中主要活性成分黄酮类及有机酸类化合物的化学特性[9],采用PLS-DA模型对炮制前后样品进行系统分析。基于上述PLS-DA中VIP>1的筛选结果[10],初步确定6个表征炮制质量差异的标志性成分。进一步结合Q-Marker“五原则”(可测性、特有性、传递性、可溯源性及有效性)[11]进行综合评价,结果得出绿原酸(峰3)、芦丁(峰10)、金丝桃苷(峰11)与异槲皮苷(峰12)色谱峰归属明确,可作为差异性成分进行后续分析。
为全面解析炮制过程化学成分的协同作用机制,本研究将上述4种差异性成分(绿原酸、芦丁、金丝桃苷、异槲皮苷)共同纳入网络药理学研究。
2.3.1山楂中炮制前后差异成分靶点预测通过Swiss Target Prediction数据库检索绿原酸、芦丁、金丝桃苷、异槲皮苷4个成分的靶点,将整理得到的靶点经Uniprot数据校准后,剔除非人类物种对应的靶点,删除无效重复靶点,将上述4个成分对应的潜在靶点合并,并以预测概率(probability,P)值>0.5为筛选条件,最终共获得178个高置信度靶点,用于后续分析。
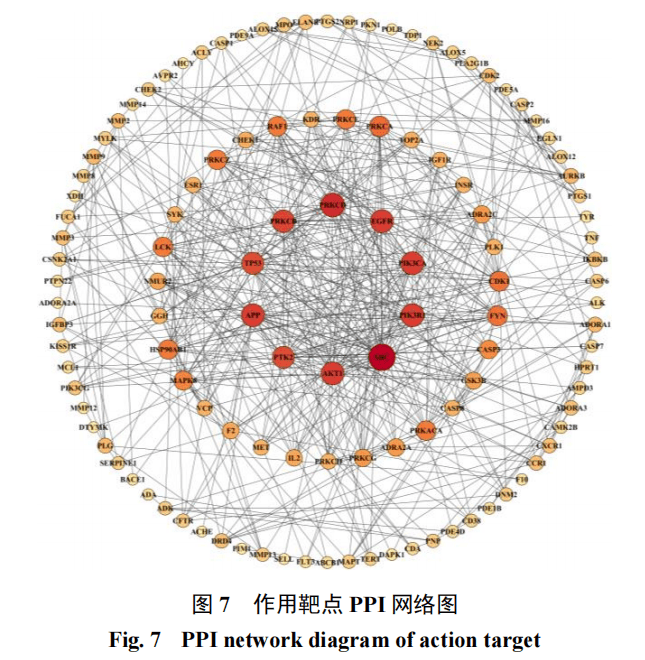
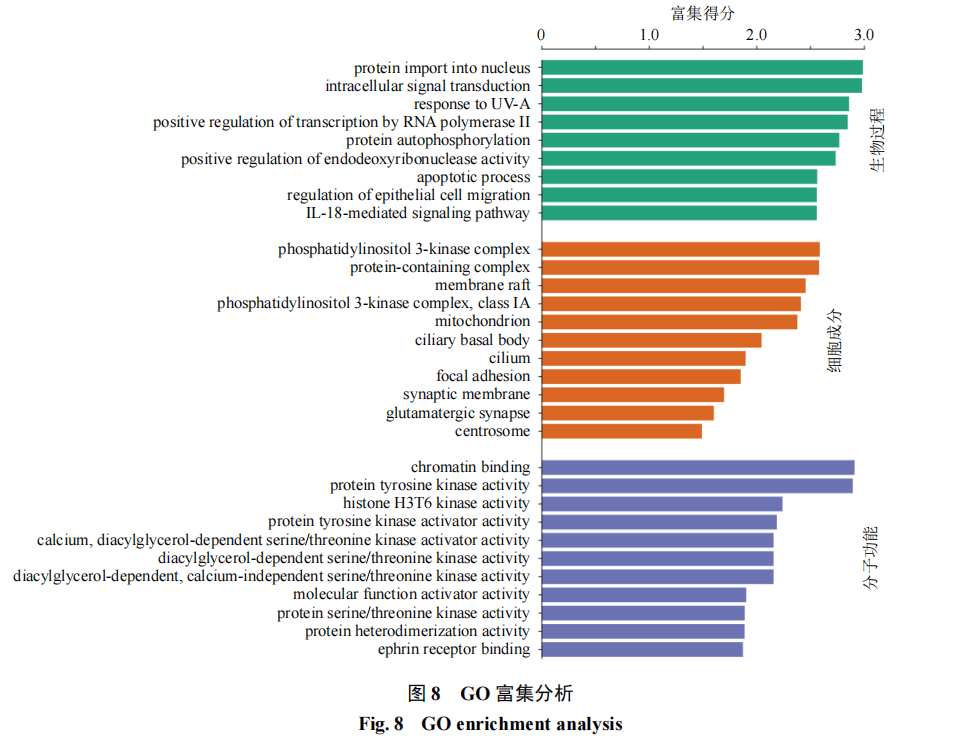
2.3.3基因本体(gene ontology,GO)富集分析和京都基因和基因组百科全书(Kyoto encyclopedia of genes and genomes,KEGG)通路分析基于DAVID数据库对筛选获得的10个核心靶点进行GO功能注释和KEGG通路富集分析。GO分析从生物过程、细胞成分和分子功能3个维度,系统揭示了靶蛋白的功能特征,共鉴定出96条显著富集的GO条目(P<0.05)。其中,生物过程相关条目占65条,其次分子功能占19条、细胞成分占12条,具体富集结果如图8所示。在生物过程方面,核心靶点主要参与蛋白质核质转运、细胞内信号转导调控、RNA聚合酶II介导的转录正向调控等;值得注意的是,靶蛋白在蛋白质自磷酸化、内切脱氧核糖核酸酶活性正调控等DNA损伤响应通路,以及上皮细胞迁移调控、白细胞介素-18(interleukin-18,IL-18)介导的信号通路等免疫调节过程中表现出显著富集特征。细胞成分分析结果显示,核心靶点主要定位于调控磷脂酰肌醇3-激酶(phosphoinositide 3-kinase,PI3K)复合体形成、膜筏结构等信号转导枢纽区域。同时,在线粒体基质、突触膜等亚细胞结构中呈现显著聚集,表明其可能参与能量代谢调控和神经突触信号传递。分子功能层面,靶蛋白表现出显著的染色质结合能力和激酶活性调控特征,具体包括Ephrin受体结合、蛋白异源二聚化活性,以及酪氨酸激酶、丝氨酸/苏氨酸激酶和组蛋白H3T6激酶等特异性磷酸化活性。这些功能特征提示化合物可能通过调控表观遗传修饰和蛋白激酶级联反应发挥生物学效应。
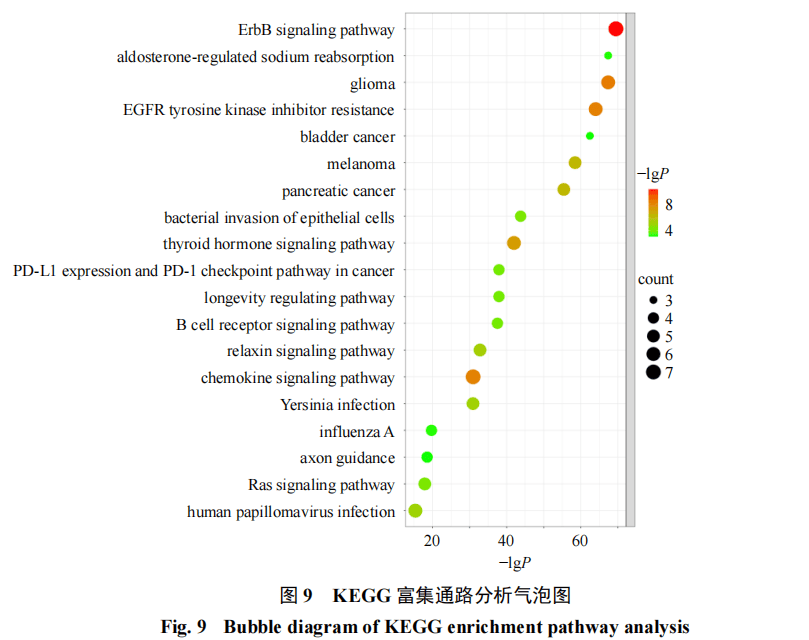
基于KEGG通路富集分析,共鉴定出112条显著性代谢通路(P<0.05)。经P值排序筛选后,重点展示了排名前20的关键代谢通路(图9)。深入分析发现,山楂炮制前后差异性成分主要通过以下3类通路发挥生物学效应。(1)肿瘤相关通路:包括ErbB信号通路、胶质瘤通路、EGFR酪氨酸激酶抑制剂耐药通路、膀胱癌通路、黑色素瘤通路、胰腺癌通路及程序性死亡配体1(programmed cell death ligand 1,PD-L1)表达与程序性死亡受体1(programmed death receptor 1,PD-1)免疫检查点通路;(2)内分泌代谢通路:涵盖醛固酮调节的钠重吸收通路和甲状腺激素信号通路;(3)基础生理调控通路:包括长寿调节通路等。
这些发现表明,178个潜在靶点可能通过协同调控肿瘤微环境、离子平衡及细胞衰老等关键生物学过程,进而干预相关疾病的病理进程,揭示了山楂炮制增效的潜在作用机制。
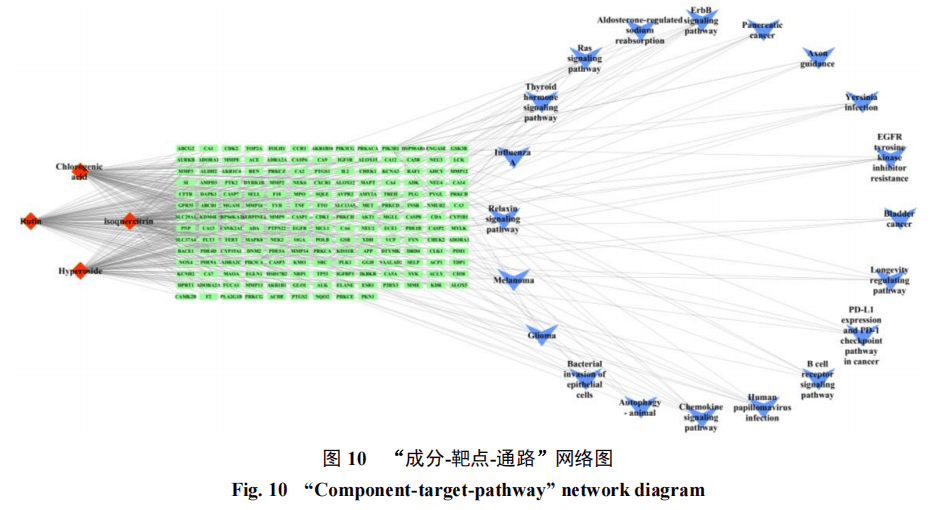
2.3.4“成分-靶点-通路”网络构建本研究采用Cytoscape 3.7.1软件构建了包含4个差异成分、178个靶点及20条关键通路的“成分-靶点-通路”网络模型(图10)。基于网络药理学分析,以化合物、靶点蛋白及信号通路的度值(degree)为筛选依据,选取网络中度值排名前7位的靶点作为介导其药效的关键靶点,分别为EGFR、PIK3CA、PIK3R1、Akt1、PRKCB、TP53、PTK2。现代研究表明,EGFR作为跨膜酪氨酸激酶受体,通过配体诱导的二聚化激活下游信号级联,在细胞增殖调控中发挥枢纽作用[12]。
PIK3CA/PIK3R1复合体作为磷脂酰肌醇3-激酶/蛋白激酶B/哺乳动物雷帕霉素靶蛋白(phosphoinositide 3-kinase/protein kinase B/mammaliantarget of rapamycin pathway,PI3K/Akt/ mTOR)信号轴的核心调控单元,其编码的p110α催化亚基与p85α调节亚基协同介导细胞代谢与存活过程,Akt1作为该通路下游效应分子,通过调控糖代谢和凋亡途径参与胃肠功能调节[13-15]。PRKCB作为丝氨酸-苏氨酸特异性蛋白激酶(PKCs)家族成员,是信号转导通路的中心分子之一,参与调节细胞增殖、分化等多种生物代谢的功能[16-17]。TP53编码的p53蛋白在细胞周期调控、DNA损伤修复、细胞凋亡及细胞代谢等过程中发挥关键作用[18]。
PTK2(FAK)是整合素介导的细胞-基质黏附和信号转导的核心调节分子。它通过整合来自细胞外基质的物理和化学信号,并将这些信号放大传递给下游多条关键信号通路(RAS/MAPK、PI3K/Akt、RHO GTPases等),从而广泛调控细胞的迁移、增殖、存活、分化和机械感应等基本生物学过程[19]。现代药理学研究证实,绿原酸具有抗菌、抗病毒及抗炎活性[20];芦丁、金丝桃苷和异槲皮苷作为黄酮类成分,均可以发挥抗炎、抗氧化、抗癌以及心脏保护与代谢性疾病干预功能[21-23]。综上,这4种成分均可能是山楂炮制前后差异性的主要活性成分,它们之间存在较高的协同作用,炮制前后的山楂可通过改变多成分、多靶点、多通路使其药理作用发生改变。预测结果与现有文献报道一致,说明该研究方法具有较高的准确率和可行性,可为山楂炮制前后的差异Q-Marker研究提供参考。
2.4.1热分析样品的制备取生山楂饮片去核粉碎后过3号筛备用,分别制备5类样品:总黄酮样品采用70%乙醇(料液比1∶20)于80℃回流提取3 h,所得滤液经蒸干、粉碎过筛后,采用硝酸铝-亚硝酸钠比色法测定其总黄酮质量分数为62.5%;有机酸样品通过蒸馏水(料液比1∶20)超声提取30 min后经冷冻干燥过筛得到,采用酸碱滴定法测定粉末中总有机酸质量分数为72.56%;鞣质样品以70%乙醇(料液比1∶20)经超声提取30 min,再于60℃恒温水浴中回流提取2 h,滤过,滤渣重复提取,合并浓缩液,干燥过筛得到,采用磷钼钨酸-干酪素比色法测定鞣质质量分数为65.68%;多糖样品通过70%乙醇(料液比1∶15)80℃回流4 h后,滤液经5倍体积95%乙醇梯度沉淀,经离心纯化、溶剂洗涤干燥过筛得,采用苯酚-硫酸法测定多糖质量分数为63.34%;醇浸出物样品按照《中国药典》2025年版四部通则2201制备山楂醇浸出物,蒸干溶剂,残渣研碎,过三号筛,备用。
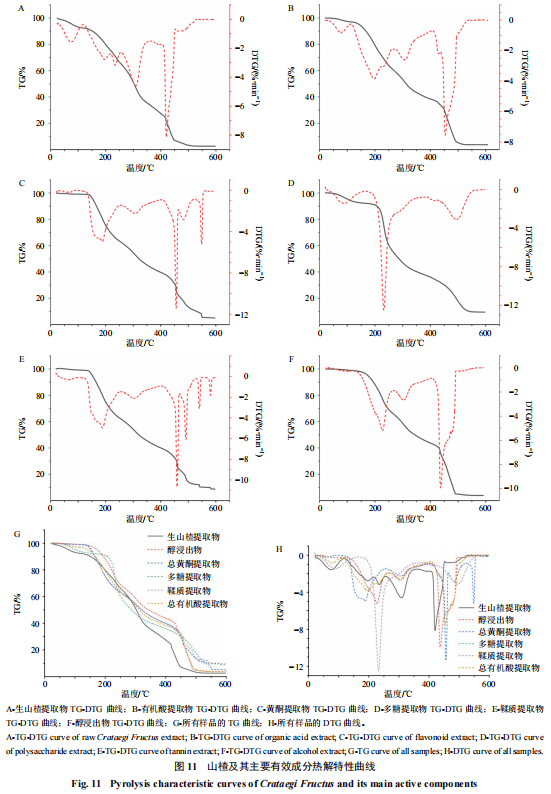
2.4.2热分析检测使用STA449-F5型热重-差热同步热分析仪,模拟空气(氮气-氧气4∶1)为载气,体积流量为60 mL/min,升温速率为10℃/min,分别取生山楂药材粉末、山楂醇浸出物、山楂总黄酮提取物、山楂多糖提取物、山楂鞣质提取物、山楂有机酸提取物(20±5)mg水平均匀分散于坩埚中,在模拟空气的条件下对其进行热解特性的研究,从室温升至600℃,每个样品平行3次实验。
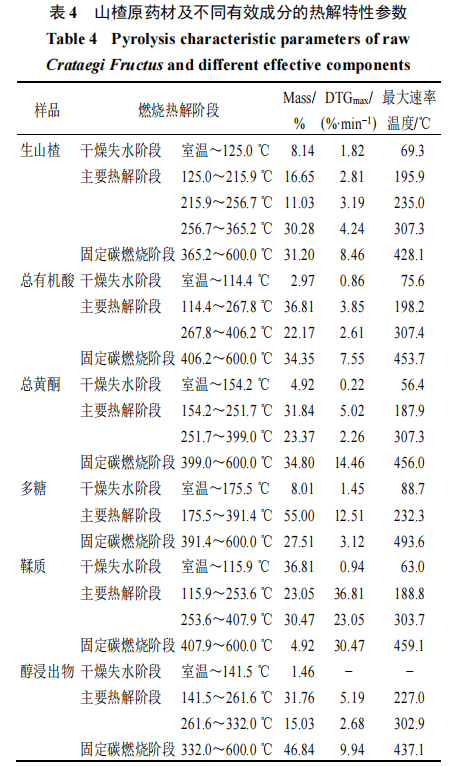
2.4.3实验结果与分析分别对热分析各样品的热解曲线)进行解析,结果如表4所示。对比生山楂粉末燃烧热解特性可知,其主要热解有3个阶段,分别为125.0~215.9℃、215.9~256.7℃、256.7~365.2℃。在215.9~256.7℃时,由TG曲线可知热失重率为11.03%,再结合DTG曲线,生山楂在235.0℃处出现强度为3.19%/min的热解燃烧阶段热失重速率峰极值。结合各组分提取物的热解特性进行深入分析发现,有机酸提取物的主要失重峰出现在198.2℃,且在114.4~267.8℃累积失重高达36.81%,这直接反映了前期筛选确定的关键Q-Marker绿原酸在此温度范围内的显著热分解特性。与此同时,总黄酮提取物在154.2~251.7℃表现出显著的热失重(31.84%),表明前期筛选确定的Q-Marker金丝桃苷和异槲皮苷在此温度范围内同样存在较高的热分解倾向。综合上述热解特性可以明确,
215.9~256.7℃是调控焦山楂关键物质基础发生预期转变的核心温度区间。在此区间内,有机酸经历显著热分解导致其含量大幅降低,这直接解释了焦山楂炮制后酸味减弱的特性。总黄酮同样在此温度区间呈现出明显的热分解倾向,其含量的适度变化与炮制后功效向消食止泻转变的预期目标相符。多糖的大量损失则可能贡献了焦山楂苦味增加的感官变化。因此,基于对有机酸、总黄酮和鞣质等在此温度区间热解行为的解析,并结合焦山楂炮制需达成的减酸增苦与增效止泻目标,初步确定焦山楂的最佳炮制温度应聚焦于215.9~256.7℃。2.5
对照品溶液的制备取绿原酸、金丝桃苷、异槲皮苷对照品适量,精密称定,加甲醇制成分别含绿原酸36.00 μg/mL、金丝桃苷14.88 μg/mL、异槲皮苷7.56 μg/mL的混合对照品溶液。
供试品溶液的制备按照“2.1.3”项下方法,取山楂粉末1 g(过三号筛),精密称定,置于50 mL锥形瓶中,加入20 mL甲醇,称定质量后超声(300 W、25℃)40 min,放冷后再次称定质量,甲醇补足减失的质量,摇匀,静置后取上清,0.22 μm微孔滤膜滤过,备用。
线性关系考察精密移取“2.5.1”下混合对照品溶液0.05、0.2、0.4、0.6、0.8、1.0、1.2 mL,分别移置于5 mL棕色量瓶中,加甲醇定容后超声(300 W、25℃),得到系列质量浓度混合对照品溶液。按照“2.5.3”项下色谱条件进样测定,以对照品溶液的质量浓度为横坐标(X),以对应峰面积为纵坐标(Y),绘制标准曲线,进行线性回归,得回归方程:绿原酸Y=23 064.0X-8 464.9,r=0.999 2,线~43.20 μg/mL;金丝桃苷Y=17 831.0X-5 617.7,r=0.999 1,线~17.86 μg/mL;异槲皮苷Y=18 503.0X-3 445.0,r=0.999 2,线~9.07 μg/mL;结果表明,各成分在各自质量浓度范围内线性关系良好。2.5.6精密度考察精密吸取“
2.5.1”项下混合对照品溶液,按“2.5.3”项下色谱条件测定,连续进样6次,记录绿原酸、金丝桃苷、异槲皮苷峰面积,计算RSD分别为1.27%、1.32%、1.14%,结果表明仪器精密度良好。2.6AHP-CRITIC法计算综合评分
,AHP)确定指标成分主观权重系数(ωAHP)山楂中的核心药效物质为黄酮类与有机酸类化合物。基于前期筛选确定的Q-Marker,本研究选取绿原酸(有机酸类代表)、金丝桃苷及异槲皮苷(黄酮类代表)作为炮制工艺优化的关键指标。根据山楂炒焦的核心目标——调整性味、增强消食止泻功效并降低胃肠刺激性,结合网络药理学与化学分析结果,明确有机酸类含量与胃肠刺激性显著相关,绿原酸通过调控IL-18等通路介导胃肠反应(图8),故作为一级指标;金丝桃苷与异槲皮苷协同调控PI3K/Akt通路(图10),共为二级指标。依据三者重要性关系(绿原酸>异槲皮苷=金丝桃苷),采用1~9标度法构建AHP判断矩阵(表5)[24]。绿原酸、异槲皮苷、金丝桃苷的ωAHP分别为0.400、0.300、0.300,最大特征根为3,一致性比例(consistency ratio,CR)值为0(<0.1),通过一致性检验,表明该ωAHP合理有效。2.6.2CRITIC
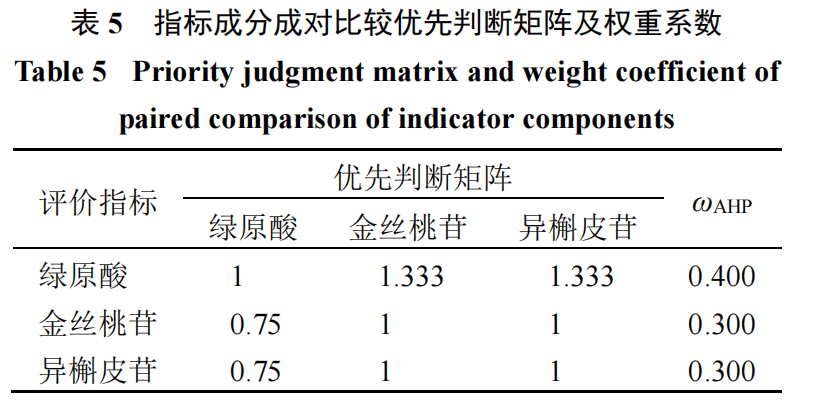
ωCRITIC)黄莉等[25]提出的CRITIC是一种客观赋权法,是一种多指标决策方法。它将得到的各项成分数据进行标准化处理,各项成分标准化值=(测量值-最小值)/(最大值-最小值)或(最大值-测量值)/(最大值-最小值)消除量纲,再计算各指标的标准差和相关系数;最后根据信息量[标准差×(1-相关系数)]计算ωCRITIC。2.6.3AHP-CRITIC法确定指标成分综合权重系数(
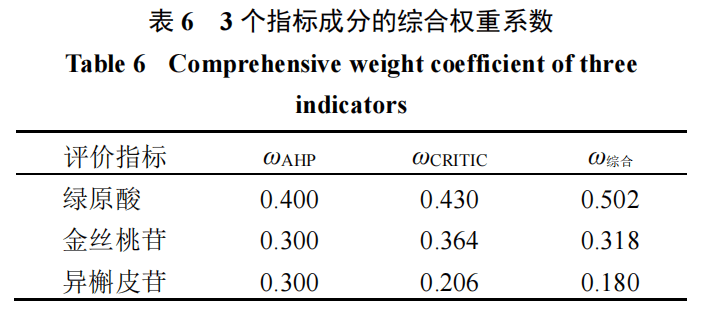
ω综合)为确保权重方法的合理性,本研究运用AHP-CRITIC法从主、客观双维度对数据予以综合赋权。计算公式为ω综合ij=ωAHPijωCRITICij/∑ωAHPijωCRITICij,ωAHPij为AHP法所得权重系数,ωCRITICij为CRITIC法所得权重系数,i与j分别对应指标i和指标j[26-27]。根据上述公式计算各指标成分的综合权重系数,结果见表6。由表6可知,绿原酸的综合权重系数最高(0.502),其次为金丝桃苷(0.318)和异槲皮苷(0.180),说明在工艺优化中绿原酸的含量变化对综合评分的影响最为显著。2.6.4综合评分计算为将多指标含量信息整合为单一评价指标以便用于后续工艺优化,建立综合评分(
Y)计算模型:Y=ω绿原酸×S绿原酸+ω金丝桃苷×S金丝桃苷+ω异槲皮苷×S异槲皮苷。其中,ω绿原酸、ω金丝桃苷、ω异槲皮苷分别为表6中的综合权重系数(0.502、0.318、0.180);Si为各成分含量的标准化值,用于消除量纲并统一变化方向,根据炮制目标,绿原酸按负向指标(S=Cmin/C),金丝桃苷与异槲皮苷按照正向指标(S=C/Cmax)进行标准化(C为实测含量,Cmax、Cmin分别为所有样品中该成分的最大、最小值)。此评分模型将作为后续工艺优化的关键响应值。2.7单因素考察
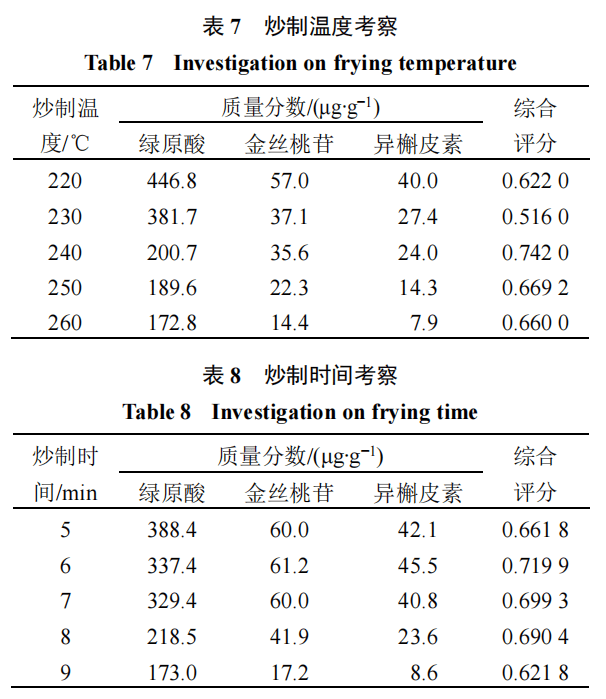
取生山楂饮片5份,每份100 g,置炒药机内,在温度为220、230、240、250、260℃下炒制8 min,取出后晾凉,即得焦山楂饮片样品。按照“2.5.3”项下方法测定绿原酸、金丝桃苷、异槲皮苷的含量,按照“2.6.3”项下确定的ω综合计算综合评分。得出240℃时综合评分最高(表7)。2.7.2炒制时间取生山楂饮片
5份,每份100 g,置炒药机内,在温度为240℃下分别炒制5、6、7、8、9 min,取出后晾凉,即得焦山楂饮片样品。按照“2.5.3”项下测定指标成分含量,确定ω综合及计算综合评分。得出6 min时综合评分最高(表8)。2.8响应面法优化焦山楂炮制工艺
取生山楂饮片适量,利用Design-Expert 8.0软件,采用中心组合设计(central combination design,CCD)法进行实验设计并在炒药机中按规定炒制,选取炒制温度(X1)和炒制时间(X2)为自变量,其编码水平均设置为−21/2、−1、0、+1、+21/2。根据CCD设计原则,软件生成了包含中心点、因子点及轴向点在内的共计13个实验点(表9)。在炒药机中按规定炒制后,以绿原酸、金丝桃苷、异槲皮苷含量的综合评分为响应值(Y)进行优化。2.8.2焦山楂响应曲面工艺优化结果分析
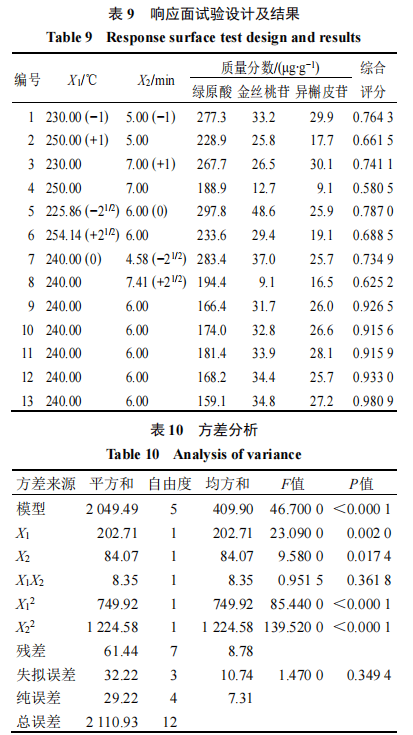
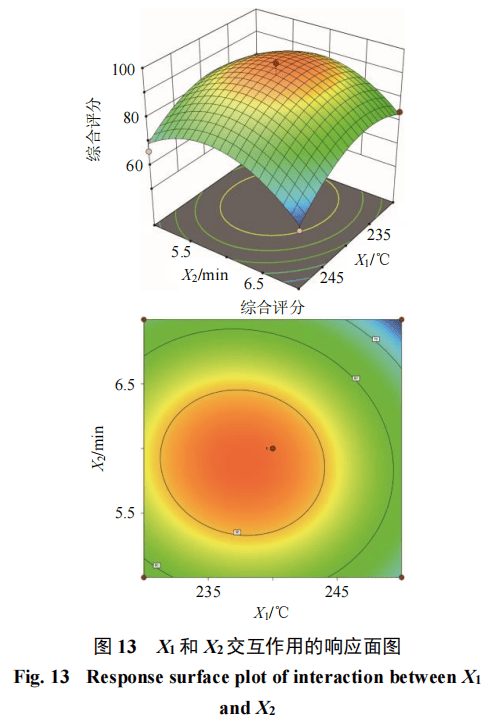
Design-Expert 8.0拟合出的X1、X2与Y的多项方程为Y=93.44-5.03X1-3.24X2-1.44X1X2-10.38X12-13.27X22,R2=0.970 9。方差分析见表10,当P<0.05为显著项、P<0.01为极显著项,模型整体具有极显著性(P<0.000 1),失拟程度不显著(P=0.349 4),表明模型能够较好的反映炒制温度(X1)、炒制时间(X2)与绿原酸、金丝桃苷和异槲皮苷的综合评分(Y)的关系,对焦山楂的炮制工艺可以进行客观准确的分析和预测。根据模型绘制炒制温度、炒制时间的交互作用3D响应面图(图13)。软件得出焦山楂最佳炮制工艺为炒制温度为238℃,炒制时间为5.89 min,综合评分为90.30分。由表9可知,各实验组的综合评分存在较大差异(0.580 5
~0.980 9分),体现了炒制温度(X1)与时间(X2)对指标成分含量的显著影响。分析可知,评分较低的第4、8组均处于高温长时的工艺条件。在此条件下,绿原酸、金丝桃苷和异槲皮苷等热敏性成分易发生分解、转化,导致其含量显著降低,进而造成综合评分下降。反之,评分较高的第9~13组处于适宜的温区与时长,既能有效促进炮制过程中的成分转化,又能避免关键成分的过度降解,使得各指标成分的含量达到最佳平衡状态。第9~13
组数据是在中心点(240℃,6 min)进行的5次重复实验,其综合评分的RSD值仅为2.48%,表明在最优工艺区域附近,该炮制工艺具有良好的重复性与稳定性,进一步验证了模型所预测最优点的可靠性。2.8.3工艺结果验证
根据响应曲面得出最优结果,结合实际操作,将焦山楂最佳炮制工艺调整为炒制温度238℃,炒制时间5.89 min(353 s),并且进行3次平行试验验证,所得平均综合评分为0.921 0分(表11),所得结果均与预测值相接近,表明焦山楂优化后的炮制工艺可行。2.9
根据优化后的焦山楂炮制工艺参数(炒制温度与炒制时间),称取适量生山楂饮片进行炒制,制备焦山楂炮制品。2.9.3电子眼分析
开启电子眼设备进行预热。预热完成后,使用24彩校正板对镜头焦距和曝光度进行校正,照明设置为顶部及底部照明。采用单一快照模式对校正板进行拍照。分别取10份生山楂饮片及其炮制品各30 g,粉碎后过筛。每份称取10 g样品粉末,均匀、整齐地平铺于样品盘上。对样品进行拍照,分析并收集电子眼色度值数据。山楂生品及其炮制品各重复测定3次,取平均值,结果见表12。表中,L*代表明度,其数值越大则越白,数值越小则越黑;a*代表从绿色到红色,正值偏红,负值偏绿;b*代表从蓝色到黄色,正值偏黄,负值偏蓝;Eab*代表的是总色差,其数值越大,颜色越浅。测定结果表明,L*、Eab*、b*值均呈现下降的趋势;a*值上升,意味着生山楂到焦山楂,其明度变暗,黄色度值显著下降,而红色度值上升,总色差下降明显,最终呈现为焦褐色,与肉眼观察一致。利用Origin 2021软件构建了山楂生品及焦山楂色度值的PCA
三维分析图(图14)。结果表明,生山楂、焦山楂在三维空间中呈现明显的空间分离,表明二者颜色特征存在显著差异。2.9.4电子鼻分析

10份生山楂饮片(S1~S10)及其炮制品(J1~J10),每份取5 g样品。将样品分别装入进样瓶中,装填至瓶身约1/3处。设置电子鼻采样参数:清洗时间120 s,采样时间60 s,气流速度1 L/min。测定前,清洗传感器至所有响应值趋于基线)。最后,将装样品的进样瓶置于仪器中进行测定,并记录所得感官数据,结果见表13。采用SIMCA 14.1软件对电子鼻获取的山楂各样品传感器响应值进行PCA。结果(图15)显示,生山楂和焦山楂能够被较为清晰地辨别开来,表明生山楂与焦山楂间的气味区别较为突出,PCA模型在对其进行区分时,表现出了较高的灵敏度以及准确性。为了进一步探明山楂及其炮制品对电子鼻中哪些传感器较为敏感,确定差异性的传感器,采用SIMCA 14.1软件对电子鼻响应值进行PLS-DA
,结果见图16。该模型累积解释能力参数R2X和R2Y分别为0.994和0.950,预测能力参数Q2为0.924,表明该模型的可解释度与预测能力良好。对PLS-DA进行200次交叉验证(图17),左侧所有绿色R2值和蓝色Q2值均低于右侧所建立模型原始值,R2及Q2与Y轴的交点分别为0.097 7和−0.306,表明所建立的模型稳定可靠且具有良好的预测性且未过拟合。由PLS-DA得分图(图16)可知,生山楂、焦山楂之间有较为明显的区分,这与PCA结果一致。在PLS-DA模型中,以VIP>
1(图18)为筛选标准,在18个传感器(C1~C18)中,C12、C6、C14、C17、C16、C18、C5、C11、C9、C4、C1这11个传感器VIP>1。这些传感器所对应的化合物的含量存在显著差异(表13、14),因此,这11个传感器可作为鉴别生山楂与焦山楂的关键指标。2.9.5电子舌分析
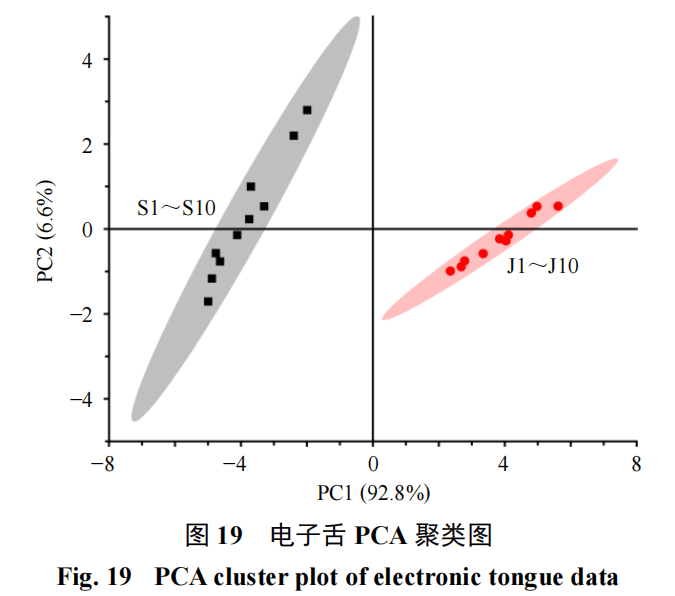
称取10批生山楂样品70 g,加入8倍量水,浸泡30 min后,加热回流提取60 min,滤过。滤渣再次加热回流提取45 min,合并2次滤液,浓缩至质量浓度为0.35 g/mL,得生山楂样品溶液。炒山楂按同法操作制备其提取液,得炒山楂样品溶液。分别取各样品滤液25 mL,浸入电子舌分析探头,采集响应信号120 s,清洗30 s,重复测定3次,记录各传感器(P1~P18)的响应信号值,结果见表15。利用Origin 2021软件构建了生山楂与焦山楂的电子舌响应值的PCA图(图19)。从PCA二维图中可得,PC1与PC2的总贡献率达到了99.40%,表明PCA模型能够高效地对原始数据进行降维处理,处理结果高度可信。在PCA图中,生山楂与焦山楂分布能够明显区分开,表明二者味道特征发生显著变化。3结论本研究通过整合指纹图谱、多元统计分析与网络药理学技术,系统筛选出山楂炮制过程中的关键

,确定绿原酸、金丝桃苷、异槲皮苷及芦丁为表征炮制差异的核心成分。鉴于芦丁在山楂生品中含量显著偏低,其作为工艺优化指标的敏感性不足,后续研究聚焦于更具代表性的绿原酸、金丝桃苷与异槲皮苷。通过热重
Q-Marker的热解行为,发现215.9~256.7℃是其动态变化的关键调控区间。绿原酸在此范围大幅降解,直接关联炮制后酸味减弱;金丝桃苷与异槲皮苷则呈现可控的热分解趋势,与其功效转化密切相关。基于此,以精准调控3类Q-Marker为目标,结合AHP-CRITIC综合赋权法建立工艺评价模型,最终优选出能有效平衡“减酸存效”的优化参数238℃下炮制5.89 min。对生山楂和焦山楂的电子感官分析表明,生山楂与工艺优化后的焦山楂在色泽、气味和味道上均存在显著差异。其中,对炮制前后气味特征的多元统计分析结果显示,C12、
C6、C14、C17、C16、C18、C5、C11、C9、C4、C1这11个传感器所响应的化合物,可作为区分生品与炮制品气味的关键指标。返回搜狐,查看更多平台声明:该文观点仅代表作者本人,搜狐号系信息发布平台,搜狐仅提供信息存储空间服务。阅读 ()